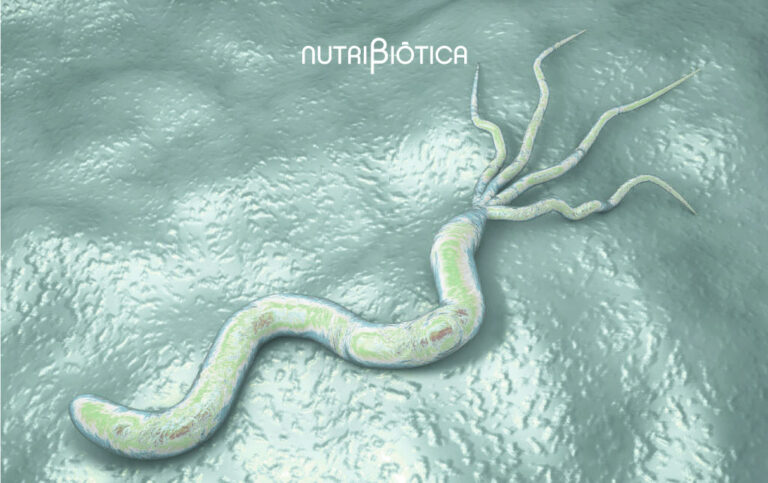
¿Trasplante fecal de microbiota o probióticos?
Se habla de microbiota y de la importancia de intervenir en ella para realizar cambios en su composición. Son varias las intervenciones que se pueden realizar. Entre ellas, destacan la alimentación, los prebióticos, los probióticos, los postbióticos, el trasplante de microbiota fecal (FMT), los antibióticos, la terapia con fagos y el CRISPR. En este artículo, la Dra. Sari Arponen analiza todos ellos, centrándose especialmente en dos: trasplante fecal y probióticos.
¿Qué vas a encontrar?
- 1 Importancia de la microbiota
- 2 Avance científico en Microbiota
- 3 Práctica clínica con Microbiota
- 4 Cómo modular la microbiota
- 5 Trasplante de microbiota fecal
- 6 Cuando se utiliza el trasplante de microbiota fecal: Clostridium difficile
- 7 ¿Es seguro hacer un trasplante de microbiota fecal?
- 8 Cómo elegir a un donante sano
- 9 Pruebas necesarias
- 10 Resultados del trasplante de microbiota fecal
- 11 Probióticos
- 12 Propiedades de los alimentos fermentados
- 13 Estudios con probióticos
- 14 Microbioterapia. Por qué no todos los probióticos son iguales.
- 15 Seguridad de los probióticos
- 16 Composición de los probióticos
- 17 La estrategia 5W1H
- 18 Conclusiones
- 19 Mantente al día de las últimas novedades en salud y microbiota con nuestra newsletter
Importancia de la microbiota
El cáncer es la segunda causa de muerte en el mundo. Aproximadamente uno de cada seis El rol del microbioma en la salud y las patologías humanas es innegable. Semana a semana, se acumulan las evidencias clínicas sobre cómo la microbiota influye en cualquier patología crónica, ya sea inflamatoria, autoinmune, neurodegenerativa o metabólica.
Si hay una enfermedad crónica, hay alteración de la microbiota: Alzheimer y Parkinson, endometriosis, síndrome de ovario poliquístico, bronquitis crónica, fibrosis quística, asma, cardiopatía isquémica, insuficiencia cardíaca, celiaquía, enfermedad inflamatoria intestinal y así en patología de cualquier órgano o sistema. ¡Hasta el ojo tiene su propia microbiota! Y las uveítis (inflamación del ojo por dentro) se han relacionado con alteraciones de la microbiota intestinal. También en procesos agudos como una infección de orina la disbiosis de la vía urinaria puede estar detrás de su aparición.

Avance científico en Microbiota
La ciencia básica no para. Todas las semanas se publican artículos sobre investigaciones en torno al tipo de microbiota que hay en cada parte del cuerpo en una enfermedad determinada. El estudio de la metabolómica también es muy interesante: los metabolitos que producen los microorganismos, por ejemplo, pueden ponernos en la pista de por qué un perfil de disbiosis determinado puede acabar participando en el proceso de aparición de una enfermedad.
La medicina moderna es la medicina de las -ómicas: microbiómica, metabolómica, proteómica, transcriptómica, epigenómica… La gran esperanza de la medicina del siglo XXI es poder aprovechar todos estos descubrimientos con un objetivo determinado: mejorar la salud de las personas y luchar contra las enfermedades crónicas que tanta calidad y cantidad de vida nos roban a los humanos modernos.
Práctica clínica con Microbiota
Si de esos conocimientos de la ciencia básica no se derivan aplicaciones para la práctica clínica, perderían parte de su sentido. El conocimiento por el conocimiento puede ser bello y estimulante. Pero si además sirve para una aplicación práctica, mejor. Así, si sabemos que en una enfermedad concreta hay alteraciones de la microbiota que participan de generar esa patología, es fácil comprender que actuando sobre esa microbiota podremos conseguir una herramienta valiosa de tratamiento.
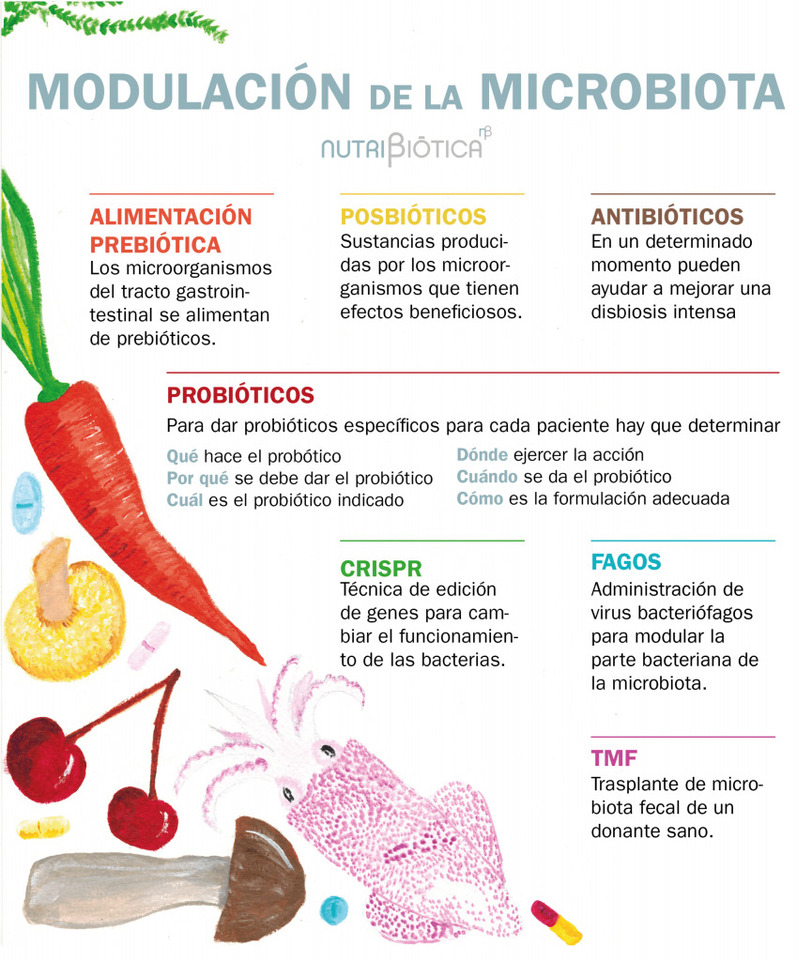
Cómo modular la microbiota
Son varias las intervenciones que se pueden realizar para cambiar la composición de la microbiota:
- Alimentación. “Somos lo que comemos”, y lo que comemos es uno de los mayores determinantes del estado de la microbiota oral e intestinal.
- Prebióticos. Se pueden obtener de la alimentación o en forma de suplemento alimentario. Los dirigidos a la microbiota intestinal son sustancias de las que se alimentan los microorganismos del tracto gastrointestinal favoreciendo el crecimiento de bacterias potencialmente beneficiosas.
- Probióticos. Son microorganismos vivos con efectos beneficiosos para el ser humanos (aunque hay probióticos de uso veterinario, en este texto nos centraremos en la salud humana; si el lector tiene una mascota con problemas de salud, quizá pueda querer modular su microbiota). Si un producto contiene probióticos y prebióticos de forma simultánea, se llama sinbiótico.
- Posbióticos. Son sustancias producidas por los microorganismos y que tienen efectos beneficiosos, como por ejemplo el butirato.
- FMT (fecal microbiota transplantation) por sus siglas en inglés es el trasplante de microbiota fecal (TMF) o “trasplante de heces” procedentes de un donante sano. El “BCT” sería una versión reducida del TMF con poblaciones seleccionadas de bacterias.
- Antibióticos, tanto farmacológicos como herbáceos, podrían utilizarse en un determinado momento para mejorar una situación de disbiosis intensa.
- Terapia con fagos. Muy poco conocida en Europa y EEUU. Se trata de administrar virus bacteriófagos para modular la parta bacteriana de la microbiota. En países como Georgia o Rusia se lleva haciendo años, pero de momento no se han trasladado sus conocimientos a nuestro medio.
- CRISPR. La técnica de edición de los genes también se ha propuesto para cambiar directamente la forma de funcionar de las bacterias de la microbiota

Alimentación
La alimentación es uno de los pilares de la configuración de la microbiota. El tipo de dieta occidental con alto consumo de azúcares, grasas industriales, productos procesados, aditivos y escasa cantidad de fibra celular y soluble hace que nuestra microbiota se desequilibre.
Una alimentación prebiótica y antiinflamatoria, rica en verduras, fruta, setas, algas, productos del mar, frutos secos, especias, aceite de oliva… es algo fundamental para el cuidado de la microbiota sobre todo intestinal y oral (descarga gratis nuestro e-book sobre «Alimentación prebiótica y antiinflamatoria», que puede servir como una propuesta básica).
De las demás intervenciones, de momento la terapia con fagos y el CRISPR no están accesibles en nuestro medio. Veamos pues qué nos pueden ofrecer el Trasplante de microbiota fecal y los probióticos.
Trasplante de microbiota fecal
Aunque el TMF se haya puesto de moda en los últimos años, en realidad es un tratamiento muy antiguo. Ya en el siglo IV en China se les daba “sopa amarilla” a las personas que tenían diarrea muy grave. Consistía en una suspensión de heces humanas y este procedimiento se describía en un manual de medicina de urgencias.
En el siglo XVI también se aconsejaban suspensiones fecales (fermentadas o frescas) o bien heces secas para las enfermedades que cursaran con diarrea. En medicina veterinaria se han llevado a cabo estas transferencias de heces con el nombre inicial de “transfaunación” desde el siglo XVII.
Cuando se utiliza el trasplante de microbiota fecal: Clostridium difficile
El primer reporte en la literatura científica moderna data de 1958 en el tratamiento de la colitis pseudomembranosa. El primer ensayo clínico con TMF se realizó en 2013 para casos de infección refractaria y recurrente por Clostridium difficile. Es una bacteria que se asocia sobre todo a tratamientos antibióticos y puede producir diarreas muy graves con inflamación extrema del intestino grueso.
De hecho, actualmente esta situación clínica es la única indicación aprobada del trasplante de microbiota fecal tanto en EEUU como en Europa, obteniéndose buenos resultados en este contexto clínico. También se han hecho estudios por ejemplo en enfermedad inflamatoria intestinal, aunque con tasas de respuesta bastante inferiores a los casos de infección por C. difficile.
Hoy en día se están haciendo ensayos clínicos en múltiples enfermedades no solo del aparato digestivo sino también extradigestivas como esclerosis múltiple, nefropatía IgA, obesidad o enfermedad de Parkinson. En algunos casos, los resultados son prometedores en un porcentaje no desdeñable de pacientes, aunque no permitirían hablar de una panacea universal para todo.
¿Es seguro hacer un trasplante de microbiota fecal?
La microbiota intestinal humana se compone de bacterias, arqueas, virus (humanos y bacteriófagos), hongos, protozoos y un tipo de bacterias de reciente descubrimiento, las CPR. No se sabe exactamente cómo tiene que ser una microbiota sana en cuanto a su fracción bacteriana. De los otros componentes aún se conoce poco su efecto sobre la salud y la enfermedad.
Además, se establecen interacciones complejas entre los microorganismos y entre los diversos dominios. Por otro lado, del material genético que forma el microbioma intestinal, hay una parte que ni siquiera se sabe a qué microorganismos pertenecen (quizá en parte a las CPR a las que se ha denominado la “materia oscura de las bacterias”).
Cuando se realiza un trasplante de microbiota fecal, se está transfiriendo el universo completo de microorganismos del donante. Hay investigadores que están preocupados por los efectos a largo plazo de los trasplantes fecales, sobre todo en las personas jóvenes.
El tratamiento de infección por Clostridium difficile es la única situación clínica en la que actualmente está aprobado el trasplante de microbiota fecal, tanto en EEUU como en Europa.
Un trasplante fecal puede ayudar a una persona que tiene un problema de salud como una enfermedad inflamatoria intestinal. Sin embargo, es posible que a los 10 o 20 años ese trasplante de microbiota fecal le provoque otra patología que el donante no padecía en el momento de realizar la donación, sino que le apareció más tarde. Quizá el problema fundamental sea que se sabe aún muy poco sobre la microbiota, y no se sabe todo lo que se ignora.
Cómo elegir a un donante sano
Para realizar el Trasplante fecal de Microbiota, la selección del donante es lo más importante. Deben realizarse múltiples estudios. Son criterios de exclusión absolutos para ser donante:
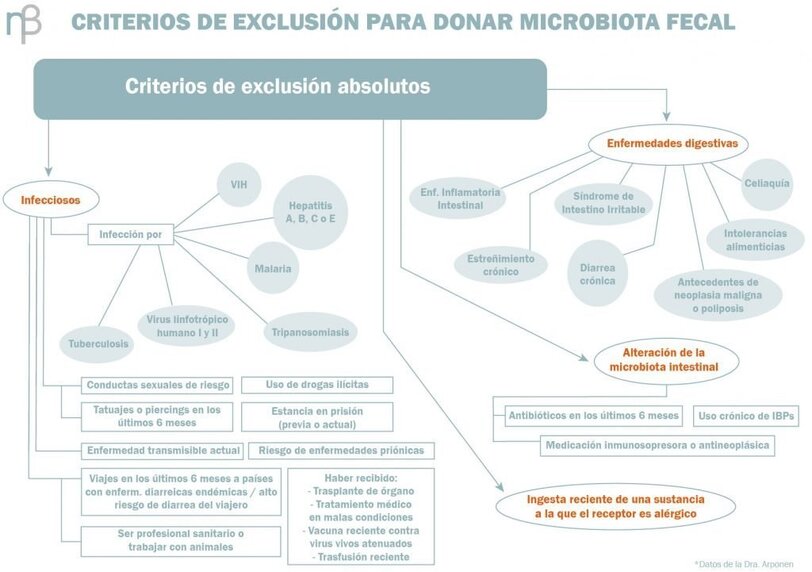

Son criterios de exclusión relativos:


Pruebas necesarias
El estudio del donante sería parecido al que se realiza a cualquier donante de órganos, además de analizar las heces con un panel mínimo de pruebas. Así, se deben realizar análisis para descartar hepatitis A aguda, hepatitis B, C o E, VIH y sífilis.
En las heces se recomienda analizar al menos sangre oculta en heces y calprotectina además de estudiar la presencia al menos de C. difficile, Giardia, rotavirus y Cryptosporidium (por antígeno), junto al examen microscópico de Cyclospora, Isospora, Cryptosporidium y parásitos. También se debe realizar cultivo bacteriano. También habría que realizar antígeno de Helicobacter pylori fecal si se va a realizar la administración por tracto gastrointestinal alto.
A un donante de heces habitual habría que realizar cribados periódicos de todas estas enfermedades o situaciones, al menos cada 3-4 meses. Sus heces se deben preparar en una batidora con un diluyente, como suero fisiológico, por ejemplo, aunque también se han usado agua, leche o yogur. Se usan entre 5-300 gramos por trasplante. Luego, la solución se puede aplicar por colonoscopia, por enema o por sonda nasogástrica. También hay algún estudio con heces encapsuladas por vía oral.
Resultados del trasplante de microbiota fecal
En principio, los resultados para la diarrea por Clostridium difficile refractaria han sido buenos. Las complicaciones han sido las derivadas del procedimiento de administración, sobre todo si es por colonoscopia. Los fallecimientos que se han comunicado parece que tuvieron que ver con la enfermedad de base o en algún caso, el procedimiento asociado al trasplante.
La difusión mediática del procedimiento ha provocado que en los últimos años haya una gran proliferación de estudios con TMF. Esta expectación ha hecho que haya personas que se hayan decidido a hacerse autotrasplantes caseros con el uso de enemas, con el riesgo que ello implica por la ausencia de controles sobre el donante.
Incluso hay páginas y vídeos en Internet con el “DIY” (Do It Yourself = Hazlo tú mismo) en Internet, con las instrucciones para el TMF casero.
En EEUU, las asociaciones de pacientes están pidiendo que se lleve a cabo más investigación en torno al trasplante de microbiota fecal y su aplicación en múltiples patologías.
Por otro lado, en EEUU se ha llegado a hablar de la “guerra de las cacas” entre los grupos de presión de la industria farmacéutica, las empresas biotecnológicas y la FDA, que actualmente considera que el trasplante de microbiota fecal es un agente biológico o un “fármaco” en investigación. Pero, ¿cómo se va a patentar algo que tenemos todos dentro de nosotros?
Por parte de asociaciones de pacientes se está pidiendo más investigación sobre el tema y la aplicación de este procedimiento en múltiples patologías. En Europa de momento sólo está aprobado en las infecciones graves refractarias y recurrentes por C. difficile.
Probióticos
Si el uso del TMF se remonta a China, los probióticos podrían considerarse aún más antiguos. La fermentación de los alimentos es un proceso muy antiguo que permitía conservarlos de forma más prolongada.
Al menos hace 8.000 años ya se hacía vino y en la antigua Babilonia se fermentaban bebidas. También los masái de forma tradicional han tomado lácteos fermentados y en Asia Central la leche fermentada de yegua y camella son alimentos tradicionales. También en la India se comen desde tiempos remotos encurtidos fermentados. En Europa también hay alimentos tradicionales como el chucrut o diversos lácteos fermentados.



Propiedades de los alimentos fermentados
En los alimentos fermentados mejora la biodisponibilidad de aminoácidos y vitaminas. Además, las propias bacterias o levaduras que pueden aparecer en el proceso pueden jugar un papel interesante en mantener una microbiota intestinal variada. En nuestra sociedad el consumo de alimentos con bacterias vivas ha pasado a ser algo residual, con sus ventajas e inconvenientes.
Fue Iliá Ilich Méchnikov, director del Instituto Pasteur, quien propuso la teoría de que las bacterias acidolácticas eran beneficiosas para la salud humana, tras observar a los campesinos búlgaros que consumían productos lácteos fermentados. Previamente su colega Henri Tissier había descrito las bifidobacterias en 1899, aunque ya a finales del siglo previo Escherich en Viena había descubierto bacterias en las heces de bebés lactantes. Méchnikov se llevó el premio Nobel en 1908 por sus descubrimientos en este campo.
Estudios con probióticos
Desde entonces ha pasado más de un siglo. En las últimas décadas ha aumentado de forma exponencial la producción de distintos tipos de probióticos, sobre todo bacterianos pero también alguna levadura. Los probióticos son “microorganismos vivos que, si se administran en suficiente cantidad, tienen efectos benéficos para la salud”.
Se han realizado miles de estudios con probióticos de diverso tipo en múltiples patologías, con resultados a veces dispares. Y es que esta definición tan amplia abarca muchos productos diferentes.
Cuando en la prensa generalista aparece una noticia con un titular del tipo: “Los probióticos no sirven para mejorar la enfermedad X” o “Los probióticos mejoran los síntomas de tal patología”, se debería revisar el artículo original y comprobar qué probiótico es el que se testó.
Microbioterapia. Por qué no todos los probióticos son iguales.
Los probióticos que se usan como microbioterapia deben ser cepas específicas, con un mecanismo de acción conocido. No es lo mismo un Lactobacillus rhamnosus LR32 que un Bifidobacterium breve B3. No tiene la misma acción un Enterococcus faecium UBEF-41 que un Lactobacillus acidophilus LA14.
Las revisiones sistemáticas que se han realizado a partir de los múltiples estudios con probióticos en los más diversos campos de la Medicina – desde la prevención de eczemas en los niños cuyas madres tomaron determinadas cepas específicas en el embarazo, hasta la prevención de complicaciones de intervenciones quirúrgicas- han permitido comprobar que una selección adecuada de las cepas de probióticos permiten actuar de forma específica y precisa según las necesidades del paciente.
Seguridad de los probióticos
En cuanto a los estudios de seguridad, el tiempo de seguimiento de los probióticos es de décadas, siendo el perfil de seguridad favorable en prácticamente todos los escenarios. Incluso en un entorno como el cuidado de pacientes críticos, hay probióticos -si se selecciona la cepa adecuada- que han demostrado ser eficaces y seguros para mejorar la duración de la estancia en UCI o reducir la tasa de ciertas infecciones asociadas a la hospitalización.
Sin embargo, los probióticos tienen la consideración de complementos alimenticios y quizá éste sea uno de los problemas. No todos los probióticos comercializados tienen la misma calidad, el origen de las cepas a menudo es difícil de averiguar, y tomar cualquier probiótico no sería lo idóneo si lo que se busca es un efecto terapéutico eficaz.



Composición de los probióticos
Las productos baratos multicepa probablemente no van a resultar dañinos pero es dudoso que se consiga un gran efecto beneficioso real en un paciente en un escenario clínico concreto. En cambio, si se hace una historia clínica cuidadosa y las pruebas complementarias adecuadas, se podrá indicar un producto más específico para el problema concreto de un paciente. No es lo mismo dar probióticos en alguien con una gastroenteritis aguda, un SIBO, o en alguien con enfermedad inflamatoria intestinal.
La estrategia 5W1H
En este sentido, resulta muy interesante la estrategia “5W1H” (del inglés What, Why, Which, Where, When, How):
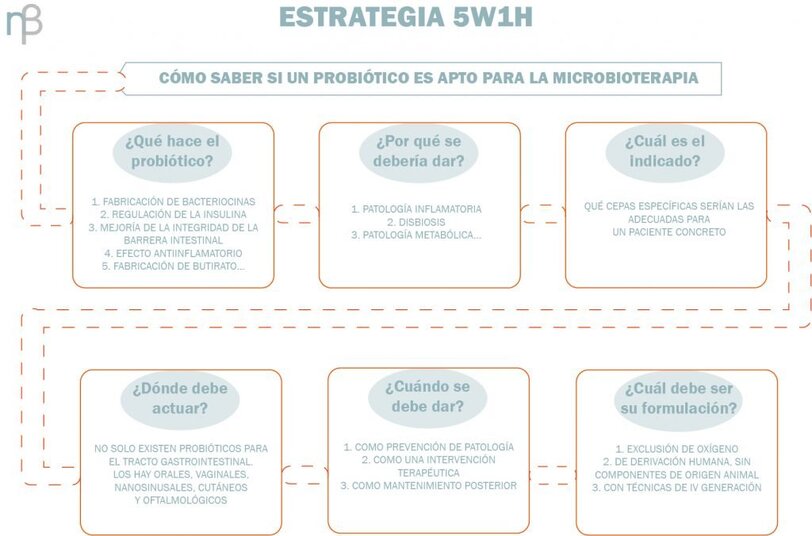

Conclusiones
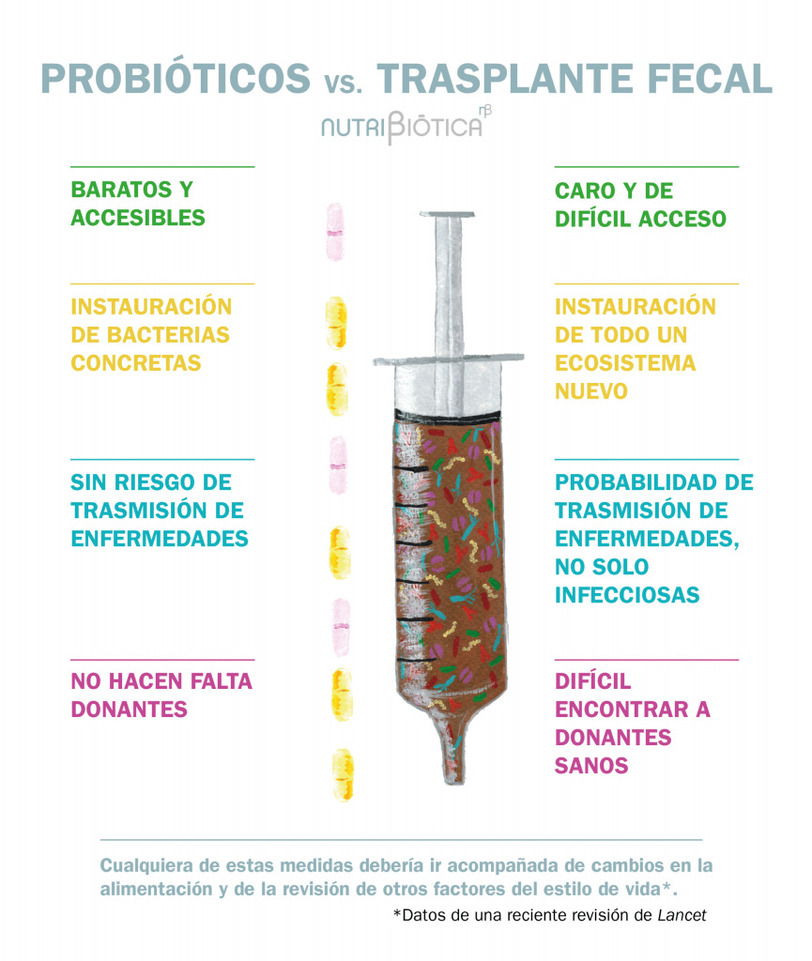
De forma resumida, en una reciente revisión de Lancet se comentaban las ventajas e inconvenientes de los probióticos, la alimentación y el trasplante de heces como estrategias de modulación de la microbiota:
Sobre la alimentación se comenta que el cambio es holístico con otras grandes ventajas en la salud. Sin embargo, a menudo hay poco cumplimiento y los efectos pueden ser muy variados.
La década que está por entrar sin duda será apasionante en lo que se refiere a nuevos descubrimientos en el mundo de la microbiota. Se desarrollarán nuevos probióticos y más ensayos y estudios con ellos, al igual que con el trasplante de heces. Sin duda, ambas intervenciones tendrán su papel en el arsenal terapéutico. No obstante, como medida única de tratamiento quizá se queden cortas.
La microbiota se modula fundamentalmente por factores ambientales: alimentación, ritmos circadianos, fármacos, tóxicos, estrés… Si una persona con una patología determinada recibe un trasplante de microbiota fecal o toma probióticos durante un tiempo pero no cambia nada más en su estilo de vida, es probable que su patología pueda recurrir al cabo de un tiempo variable. Cualquiera de estas medidas debería ir acompañada de cambios en la alimentación y revisión de otros factores del estilo de vida que ayuden a mantener la mejoría que se pueda haber logrado.
Un maestro me dijo una vez: “En Medicina hay que conocer lo último, pero aplicar lo penúltimo”. Si le añadimos el “Vamos muy deprisa pero no sabemos a dónde”, quizá podamos tener una orientación que nos permita transitar con cierta seguridad y prudencia en este apasionante mundo de la microbiota.


La Dra Sari Arponen es licenciada en Medicina y Cirugía por la Universidad de Murcia (2001), Doctora Cum Laude en Ciencias Biomédicas por la Universidad Complutense de Madrid, especialista en Medicina Interna por el Hospital Universitario de la Princesa de Madrid, profesora universitaria y experta en microbiota.
Tiene un máster en Enfermedades Infecciosas y otro en VIH, un posgrado de tres años en Psiconeuroinmunología Clínica por la Universidad de la Pontificia de Salamanca y es Experta Universitaria en Nutrición.
Ha trabajado como internista en varios hospitales de la Comunidad de Madrid, con dedicación especial a las enfermedades infecciosas.
Ha realizado más de un centenar de cursos de formación continuada acreditados y ha participado activamente en diversos ensayos clínicos y estudios multicéntricos. Desde hace unos años, se ha centrado en el estudio y la práctica de la Medicina Evolucionista y de la Psicoinmunología clínica. Tras casi veinte años de experiencia clínica en la sanidad pública española, en la actualidad se dedica a la formación y divulgación en el ámbito de la microbiota y la medicina del estilo de vida.

- #NBlog
- Puede que también te interese
Suscríbete a nuestra newsletter y sé el primero en enterarte de todas nuestras ofertas y promociones.